카티스템 허가 후 첫 해외 설명회
일본 바이오 아시아서 임상 결과 및 시장 진출 계획 등 발표
허가 계기로 카티스템 해외 홍보 및 시장 개척에 박차

메디포스트(대표: 양윤선)는 ‘카티스템’의 식약청 품목허가 취득 이후 처음으로 국제 컨퍼런스에 참가, 임상 유효성과 글로벌 시장 진출 계획 등을 발표했다.
메디포스트는 1월 31일~2월 1일 이틀간 일본 오사카에서 열린 ‘제 9회 바이오 아시아(Bio Asia)’에서 해외 제약, 바이오 기업 관계자들을 대상으로 ‘카티스템’에 관해 설명하고, 이 중 10여 곳과 1:1 미팅도 가졌다. 이번 행사에는 개최국인 일본을 비롯해 중국, 싱가포르 등 아시아 주요 국가와 미국, 유럽 등 전 세계 유명 제약사 및 연구소, 정부기관에서 참여했으며, 한국 기업으로는 메디포스트가 유일하게 참가했다.
‘바이오 아시아’는 미국 생명공학산업기구(Biotechnology Industry Organization, BIO) 주관으로 매년 일본에서 열리고 있으며, ‘바이오 U.S.’, ‘바이오 유럽’과 함께 바이오 분야 세계 3대 행사로 꼽히고 있다. 이와 관련 메디포스트 관계자는 “품목허가를 받은 이후 해외 의약계의 관심이 크게 높아졌고, 이번 발표회를 계기로 해외에서의 카티스템 홍보 및 시장 개척에 더욱 박차를 가할 것”이라고 말했다.
메디포스트는 별도의 임상시험 없이 우리나라 식약청 품목허가만으로 카티스템 의 판매가 가능한 아시아와 동유럽, 중남미 지역 국가들을 대상으로 직수출을 추진하고 있다.
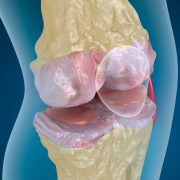
한편 카티스템 은 퇴행성 혹은 반복적 외상으로 인한 골관절염 환자의 무릎 연골 결손 치료제로, 지난 19일 식약청 품목허가를 받았으며 규격제품화와 대량 생산이 가능한 세계 최초의 동종 줄기세포치료제로 관심을 모으고 있다.
 제대혈 보관/계약 문의 :
제대혈 보관/계약 문의 :