카티스템 미국 임상 투여 완료
연골 재생 줄기세포 치료제, 임상 1/2a상 피험자 12명 투여 종료
향후 1년간 유효성 추적관찰 예정
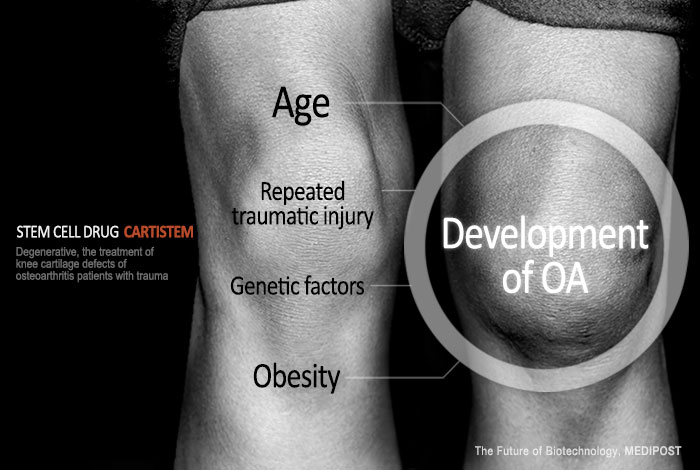
메디포스트(대표: 양윤선)는 미국에서 진행 중인 연골 재생 줄기세포 치료제 ‘카티스템(CARTISTEM)’의 제1/2a상 임상 투여를 모두 완료했다고 5월 29일 밝혔다. 메디포스트는 5월 28일(한국날짜) 시카고 러시대학교병원에서 연골 결손 환자를 대상으로 ‘카티스템’ 제1/2a상 임상시험의 마지막 피험자 투여를 실시했다.
메디포스트는 2011년 2월 미국 식품의약국(FDA)의 승인을 받아, 러시대학교병원과 보스턴 하버드대 브리엄여성병원에서 총 12명의 피험자를 대상으로 ‘카티스템’의 제1/2a상 임상시험을 진행해 왔다. 메디포스트는 앞으로 약 1년간 ‘카티스템’의 유효성을 추적 관찰한 후, 평가 결과를 분석해 FDA에 제출할 예정이다.
이와 관련, 오원일 메디포스트 부사장은 “미국 정형외과 분야 최고 권위의 병원 2곳에서 ’카티스템’의 임상 투여를 성공적으로 마쳤다”며, “담당 의사와 초기 피험자들의 만족도가 매우 높아 좋은 임상 결과를 얻을 수 있을 것으로 기대한다”고 말했다. 실제로 임상에 참여한 브리엄여성병원의 A. 고몰(Gomoll) 교수는 최근 미국 ABC 방송과의 인터뷰에서 “’카티스템’ 시술은 다른 치료에 비해 회복 기간이 짧고 튼튼한 연골이 재생된다”고 설명했다.
러시대학교병원의 브라이언 J. 콜(Brian J. Cole) 교수도 임상 중 현지 방송에 출연해 “기존 연골 재생 치료법이 만족스러운 효과를 거두지 못했던 반면 ‘카티스템’은 장기적으로 유효성을 기대할 수 있다”고 평가한 바 있다.
‘카티스템’은 퇴행성 또는 반복적 외상으로 인한 골관절염 환자의 무릎 연골 결손 치료제로, 2012년 한국에서 식약처 품목허가를 취득한 세계 최초의 동종 줄기세포 치료제이다.‘카티스템’은 현재 국내에서는 2천여 건의 시술이 이뤄졌으며, 매 분기 시술 건수가 점진적으로 증가하면서 국내 줄기세포 치료제의 상업적 성공 가능성을 보여주고 있다.
 제대혈 보관/계약 문의 :
제대혈 보관/계약 문의 :